Le sostanze estremamente preoccupanti (SVHC) del REACH e la "Candidate List" ECHA / Update Giugno 2024
ID 2988 | 30.06.2024 / Documento completo allegato
L'elenco delle sostanze estremamente preoccupanti (SVHC) candidate all’autorizzazione è pubblicato dall'ECHA in conformità all'art. 59 p. 10, del regolamento (CE) n. 1907/2006 (REACH).
- Perossido di bis(α,α-dimetilbenzile)
______
Update 30.06.2024
ECHA: Update candidate list 27.06.2024
______
Cos'è la "Candidate list" ECHA?
La "Candidate list" dell'ECHA è una lista di sostanze estremamente preoccupanti (SVHC - Substances of Very High Concern identification) che l'Agenzia Europea delle sostanze chimiche (ECHA), ha l'obbligo di pubblicare e aggiornare.
La Sezione 15 della SDS (allegato II Regolamento REACH) deve includere informazioni sulle norme e legislazione su salute, sicurezza e ambiente specifiche per le sostanze (Informazioni sulla Regolamentazione legislazione dell'Unione Europea) delle "sostanze candidate" come sostanze estremamente preoccupanti (SVHC) ai sensi dell'articolo 59, paragrafo 10, del Regolamento REACh.
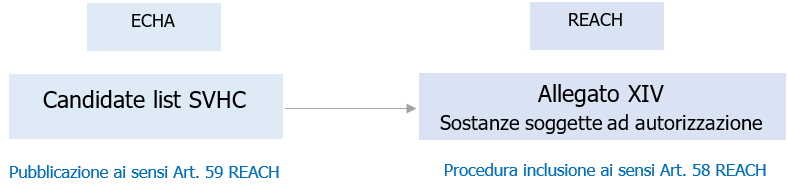
Fig. 1 - Relazione tra sostanze in Candidate list SVHC ECHA e Allegato XIV REACH
...
Articolo 57 Sostanze da includere nell'allegato XIV
Le sostanze seguenti possono essere incluse nell'allegato XIV secondo la procedura di cui all'articolo 58:
a) le sostanze che rispondono ai criteri di classificazione nella classe di pericolo cancerogenicità, categoria 1A o 1B, di cui al punto 3.6 dell'allegato I del regolamento (CE) n. 1272/2008;
b) le sostanze che rispondono ai criteri di classificazione nella classe di pericolo mutagenicità sulle cellule germinali, categoria 1A o 1B, di cui al punto 3.5 dell'allegato I del regolamento (CE) n. 1272/2008;
c) le sostanze che rispondono ai criteri di classificazione nella classe di pericolo tossicità per la riproduzione, categoria 1A o 1B, effetti nocivi sulla funzione sessuale e la fertilità o sullo sviluppo di cui al punto 3.7 dell'allegato I del regolamento (CE) n. 1272/2008;
d) le sostanze che sono persistenti, bioaccumulabili e tossiche, secondo i criteri di cui all'allegato XIII del presente regolamento;
e) le sostanze che sono molto persistenti e molto bioaccumulabili, secondo i criteri di cui all'allegato XIII del presente regolamento;
f) le sostanze come quelle aventi proprietà che perturbano il sistema endocrino o quelle aventi proprietà persistenti, bioaccumulabili e tossiche o molto persistenti e molto bioaccumulabili, che non rispondono ai criteri di cui alle lettere d) o e), per le quali è scientificamente comprovata la probabilità di effetti gravi per la salute umana o per l'ambiente che danno adito ad un livello di preoccupazione equivalente a quella suscitata dalle altre sostanze di cui alle lettere da a) a e), e che sono identificate in base ad una valutazione caso per caso secondo la procedura di cui all'articolo 59.
Articolo 58 Inclusione di sostanze nell'allegato XIV
1. Ogniqualvolta si decide di includere nell'allegato XIV una o più sostanze di cui all'articolo 57, la decisione è assunta secondo la procedura di cui all'articolo 133, paragrafo 4. Per ogni sostanza, è precisato quanto segue:
a) l'identità della sostanza, come specificato nell'allegato VI, punto 2;
b) la o le proprietà intrinseche della sostanza di cui all'articolo 57;
c) disposizioni transitorie:
i) la data o le date a partire dalle quali l'immissione sul mercato e l'uso della sostanza sono vietati, salvo qualora sia rilasciata un'autorizzazione (in seguito denominata: «data di scadenza»), che dovrebbero tener conto, se del caso, del ciclo di produzione specificato per tale uso;
ii) una o più date precedenti di almeno diciotto mesi la o le date di scadenza, entro cui devono pervenire le domande se il richiedente intende continuare a utilizzare la sostanza o a immetterla sul mercato per determinati usi dopo la o le date di scadenza; la prosecuzione di tali usi è autorizzata dopo la data di scadenza fintantoché non è assunta una decisione sulla domanda di autorizzazione;
d) se del caso, i periodi di revisione per taluni usi; e) gli eventuali usi o categorie di usi esentati dall'obbligo d'autorizzazione e le eventuali condizioni di tali esenzioni.
2. Gli usi o categorie di usi possono essere esentati dall'obbligo di autorizzazione, a condizione che il rischio sia adeguatamente controllato, in base alla vigente normativa comunitaria specifica che impone prescrizioni minime per l'uso della sostanza connesse alla protezione della salute umana o alla tutela dell'ambiente. Nello stabilire tali esenzioni, si tiene conto, in particolare, della proporzionalità del rischio per la salute umana e per l'ambiente connessa alla natura della sostanza, come nel caso in cui il rischio è modificato dalla forma fisica.
3. Prima di assumere una decisione sull'inclusione di sostanze nell'allegato XIV, l'Agenzia, tenuto conto del parere del comitato degli Stati membri, raccomanda sostanze prioritarie da includere, precisando per ogni sostanza gli elementi di cui al paragrafo 1. Di norma, sono considerate prioritarie le sostanze:
a) che hanno proprietà PBT o vPvB; o
b) il cui uso è fortemente dispersivo; o
c) che sono prodotte ad alti volumi.
Il numero di sostanze incluse nell'allegato XIV e le date fissate a norma del paragrafo 1 tengono conto anche della capacità dell'Agenzia di evadere le domande nei termini previsti. L'Agenzia redige la prima raccomandazione relativa a sostanze prioritarie da includere nell'allegato XIV entro il 1o giugno 2009. L'Agenzia redige ulteriori raccomandazioni, quantomeno ogni due anni, nell'ottica di includere altre sostanze nell'allegato XIV.
4. Prima di trasmetterla alla Commissione, l'Agenzia pubblica la raccomandazione sul suo sito web, indicando chiaramente la data di pubblicazione, nel rispetto delle disposizioni degli articoli 118 e 119 sull'accesso alle informazioni. Essa invita tutte le parti interessate a presentare, entro i tre mesi successivi alla data di pubblicazione, osservazioni riguardanti in particolare gli usi che dovrebbero essere esentati dall'obbligo d'autorizzazione. L'Agenzia aggiorna la sua raccomandazione tenendo conto delle osservazioni ricevute.
5. Fatto salvo il paragrafo 6, una volta inclusa nell'allegato XIV, una sostanza non è assoggettata a nuove restrizioni secondo la procedura di cui al titolo VIII in relazione ai rischi che l'uso della sostanza in quanto tale, come componente di una miscela o incorporata in un articolo, comporta per la salute umana o per l'ambiente a motivo delle proprietà intrinseche di cui all'allegato XIV.
6. Una sostanza elencata nell'allegato XIV può essere assoggettata a nuove restrizioni secondo la procedura di cui al titolo VIII in relazione ai rischi che la presenza della sostanza in uno o più articoli comporta per la salute umana o per l'ambiente.
7. Le sostanze per le quali sono stati vietati tutti gli usi a norma del titolo VIII o di altre normative comunitarie non sono incluse nell'allegato XIV o ne sono depennate.
8. Le sostanze che in base a nuove informazioni non risultano più rispondere ai criteri di cui all'articolo 57, sono depennate dall'allegato XIV secondo la procedura di cui all'articolo 133, paragrafo 4.
Articolo 59 Identificazione delle sostanze di cui all'articolo 57
1. Ai fini dell'identificazione delle sostanze che rispondono ai criteri di cui all'articolo 57 e della definizione di un elenco di sostanze candidate all'eventuale inclusione nell'allegato XIV, si applica la procedura di cui ai paragrafi da 2 a 10 del presente articolo. L'Agenzia indica, in questo elenco, le sostanze che figurano nel programma di lavoro di cui all'articolo 83, paragrafo 3, lettera e).
2. La Commissione può chiedere all'Agenzia di predisporre un fascicolo, a norma dei pertinenti punti dell'allegato XV, per le sostanze che, a suo giudizio, rispondono ai criteri di cui all'articolo 57. Il fascicolo può essere limitato, se del caso, a un riferimento a una voce dell'allegato VI, parte 3, del regolamento (CE) n. 1272/2008.; L'Agenzia mette il fascicolo a disposizione degli Stati membri.
3. Ogni Stato membro può predisporre un fascicolo a norma dell'allegato XV per le sostanze che, a suo giudizio, rispondono ai criteri di cui all'articolo 57 e trasmetterlo all'Agenzia. Il fascicolo può essere limitato, se del caso, a un riferimento a una voce dell'allegato VI, parte 3, del regolamento (CE) n. 1272/2008. L'Agenzia mette il fascicolo a disposizione degli altri Stati membri entro trenta giorni dalla ricezione.
4. L'Agenzia pubblica sul suo sito web un avviso dell'avvenuta predisposizione a norma dell'allegato XV di un fascicolo per una sostanza. L'Agenzia invita tutte le parti interessate a trasmetterle osservazioni entro un termine stabilito.
5. Entro sessanta giorni dalla messa a disposizione, gli altri Stati membri o l'Agenzia possono formulare osservazioni sull'identificazione della sostanza in relazione ai criteri di cui all'articolo 57 nel fascicolo trasmesso all'Agenzia.
6. Se non riceve o non formula osservazioni, l'Agenzia può includere la sostanza nell'elenco di cui al paragrafo 1. Essa può includere la sostanza nelle raccomandazioni che formula a norma dell'articolo 58, paragrafo 3.
7. Qualora vengano formulate o ricevute osservazioni, l'Agenzia rinvia il fascicolo al comitato degli Stati membri entro quindici giorni dallo scadere del periodo di sessanta giorni di cui al paragrafo 5.
8. Se, entro trenta giorni da tale rinvio, il comitato degli Stati membri giunge ad un accordo unanime sull'identificazione, l'Agenzia include la sostanza nell'elenco di cui al paragrafo 1. Essa può includere tale sostanza nelle raccomandazioni che formula a norma dell'articolo 58, paragrafo 3.
9. Se il comitato degli Stati membri non riesce a giungere a un accordo unanime, entro tre mesi dalla ricezione del parere del comitato degli Stati membri la Commissione prepara un progetto di proposta relativa all'identificazione della sostanza in questione. La decisione definitiva sull'identificazione della sostanza è assunta secondo la procedura di cui all'articolo 133, paragrafo 3.
10. Non appena è stata assunta una decisione sull'inclusione di una sostanza l'Agenzia pubblica e aggiorna senza indugio sul suo sito web l'elenco di cui al paragrafo 1.
Il riferimento ufficiale è rappresentato dal sito dell’Agenzia Europea delle sostanze chimiche (ECHA) che è tenuta a pubblicare e aggiornare il citato elenco:
...
(vedi allegato)
L'Istituto Superiore di Sanità (ISS) predispone e gestisce la banca dati di modelli di schede di dati di sicurezza (SDS) di sostanze chimiche come supporto per tutti gli attori che hanno obbligo, ai sensi del Regolamento 1907/2006 (REACH), di trasmettere al destinatario della sostanza una SDS a norma dell'Allegato II del citato regolamento. Scopo di questo progetto è quello di uniformare ed elevare la qualità delle SDS e fornire anche un punto di riferimento per l’attività di vigilanza.
Le SDS della Banca dati, non hanno alcun valore legale ma rappresentano modelli da utilizzare, modificare ed integrare da parte di tutti coloro a cui spetta l’obbligo di redigerle al fine di adattarle alle proprie esigenze assumendone la piena responsabilità.
La banca dati include informazioni relative alla classificazione armonizzata delle sostanze con riferimento all’allegato VI del Reg. CLP (sez. 2.1 della SDS) e alle norme e legislazione su salute, sicurezza e ambiente specifiche per le sostanze che vanno incluse nella sez. 15 (Informazioni sulla Regolamentazione legislazione dell'Unione Europea).
Identificazione delle sostanze estremamente problematiche
Le sostanze che potrebbero avere effetti gravi e spesso irreversibili sulla salute umana e sull’ambiente possono essere identificate come sostanze estremamente preoccupanti (SVHC).
Se identificata come SVHC, la sostanza sarà:
1. aggiunta all’elenco di sostanze candidate
2. aggiunta definitiva inclusione nell’elenco delle sostanze soggette ad autorizzazione.
Partecipazione alla consultazione pubblica
Gli Stati membri o l’Agenzia europea per le sostanze chimiche (ECHA), su richiesta della Commissione europea, possono proporre che una sostanza sia identificata come SVHC preparando un fascicolo in conformità delle prescrizioni di cui all’allegato XV del regolamento REACH. Le relazioni ai sensi dell’allegato XV possono essere reperite selezionando il pulsante “Details” (dettagli) nella tabella che elenca le sostanze proposte. Tutte le parti interessate sono invitate a presentare osservazioni su tali relazioni nel corso della consultazione pubblica.
Formulazione di osservazioni
L’identificazione di SVHC si basa sulle proprietà pericolose di una sostanza. Sono particolarmente gradite le osservazioni su quanto segue:
- identità della sostanza (ossia denominazione della sostanza/numero CE/numero CAS/struttura molecolare, ecc.);
- proprietà PBT o vPvB e proprietà che danno adito a un livello di preoccupazione equivalente.
Le proposte di SVHC sulla base di classificazioni ed etichettature armonizzate (CLH) di cui al regolamento CLP non possono essere messe in discussione nel processo di identificazione della SVHC. Pertanto, le osservazioni che pongono in discussione la classificazione e l’etichettatura armonizzate non saranno prese in considerazione in tale contesto.
Anche le osservazioni e le ulteriori informazioni relative a usi, volumi per uso, esposizione, alternative e rischi della sostanza sono accolte favorevolmente da tutte le parti interessate. Queste ulteriori informazioni saranno utilizzate non per confermare l’identificazione di SVHC ma per aiutare l’ECHA a decidere, durante la fase successiva del processo di autorizzazione, se la sostanza debba essere raccomandata per l’inclusione nell’elenco delle sostanze soggette ad autorizzazione. I fascicoli di registrazione costituiscono comunque la principale fonte di informazioni per raccomandare il passaggio di sostanze dall’elenco di sostanze candidate all’elenco delle sostanze soggette ad autorizzazione.
Lo Stato membro proponente le sostanze SVHC o l’ECHA risponderà alle eventuali osservazioni ricevute. Le osservazioni riguardanti l’identificazione della sostanza come SVHC verranno inoltrate al comitato degli Stati membri, che valuterà se la sostanza debba essere identificata come SVHC.
Riservatezza
Generalmente, le osservazioni fornite non sono considerate riservate e saranno messe a disposizione del pubblico sul sito web dell’ECHA. Esiste, tuttavia, la possibilità di allegare informazioni riservate. In questo caso, la persona/parte che presenta le osservazioni deve giustificare il motivo per cui le informazioni sono considerate riservate fornendo le spiegazioni del caso. Dette informazioni riservate saranno utilizzate solo dall’ECHA, compresi i suoi comitati, le autorità competenti degli Stati membri proponenti e la Commissione europea.
L’ECHA sarebbe grata se, ove possibile, le parti interessate presentassero le proprie osservazioni in inglese. Si noti che è responsabilità della parte interessata garantire che nessuna informazione riservata sia inclusa nella versione pubblica delle osservazioni (fra cui il nome dell’organizzazione dell’utente/i titoli dei file allegati, ecc.). Nelle osservazioni si invita anche a fare riferimento al numero di pagina della relazione ai sensi dell’allegato XV (per esempio, pag. 12 la conclusione riguardante ...). Le osservazioni pervenute dopo il termine stabilito non saranno prese in considerazione.
In allegato una SDS (Acido arsenico) estratta dalla Banca Dati SDS dell'ISS, sostanza in candidate list ECHA, al punto 15:
Acido Arsenico SVHC Numero CE 231-901-9
SEZIONE 15: Informazioni sulla regolamentazione
15.1. Norme e legislazione su salute, sicurezza e ambiente specifiche per la sostanza o la miscela Regolamenti UE
Autorizzazioni e/o Restrizioni d’uso:
Autorizzazioni: Sostanza inclusa nell’allegato XIV del Reg. 1907/2006 (Reg. 895/2014) [data entro cui devono pervenire le domande: 22 febbraio 2016; data di scadenza: 22 agosto 2017]
Restrizioni d’uso: - Sostanza inclusa nell’allegato XVII del Reg. 1907/2006 voce n° 19 – Composti dell’arsenico - Sostanza inclusa nell’allegato XVII del Reg. 1907/2006 voce n° 28 – sostanze cancerogene (Regolamento 109/2012).
Lista SVHC: Sostanza inclusa nella lista SVHC in data 19/11/2011 in quanto cancerogena (art. 57a)
Altri Regolamenti UE
L’arsenico e suoi composti sono vietati nei prodotti cosmetici (Regolamento 1223/2009, All. II n. 43).
L’uso della sostanza nella formulazione dei tatuaggi e del trucco permanente è vietato in quanto la sostanza è presente nell’Allegato II del Regolamento 1223/2009 (sostanze vietate nei prodotti cosmetici) (Risoluzione ResAP(2008)1 del Consiglio di Europa).
Sostanza coperta dalla Direttiva 2006/11/CE concernente l'inquinamento provocato da certe sostanze pericolose scaricate nell'ambiente idrico della Comunità e dalla Direttiva 2000/60/CE concernente l’azione comunitaria in materia di acque. La direttiva 96/82/CE (Direttiva Seveso II), sul controllo dei pericoli di incidenti rilevanti connessi con determinate sostanze pericolose, definisce per questa sostanza quantità limite specifiche. La quantità limite per l’applicazione dell’articolo 9 [Rapporto di sicurezza] è 100 kg (Dir. 96/82/CE Allegato I, parte 1).
Norme Italiane
Restrizioni professionali: Decreto Legislativo 4 agosto 1999, n. 345 relativo alla protezione dei giovani sul lavoro.
Decreto Legislativo 26 marzo 2001, n. 151 riguardante le lavoratrici gestanti, puerpere e in allattamento.
15.2. Valutazione della sicurezza chimica
Considerare la valutazione della sicurezza chimica tenendo conto soprattutto delle proprietà chimico-fisiche, del modo e le circostanze di utilizzo della sostanza o del preparato.
...
Matrice Revisioni
| Rev. | Data | Oggetto | Autore |
| 4.0 | 30.06.2024 | ECHA: Update candidate list 27.06.2024 | Certifico Srl |
| 3.0 | 23.01.2024 | ECHA: Update candidate list 23.01.2024 | Certifico Srl |
| 2.0 | 14.06.2023 | ECHA: Update candidate list 14.06.2023 | Certifico Srl |
| 1.0 | 17.01.2023 | ECHA: Update candidate list 17.01.2023 |
Certifico Srl |
| 0.0 | 10.06.2022 | ECHA: Update candidate list 10.06.2022 | Certifico Srl |
Collegati
Regolamento (CE) n. 1907/2006 REACH
Elenco sostanze soggette ad autorizzazione REACH (Allegato XIV)
ECHA: Update candidate list 10.07.2017
ECHA: Update candidate list 20.12.2017
ECHA: Update Candidate list 15.01.2018
ECHA: Update Candidate List 27.06.2018
ECHA: Update Candidate list 15.01.2018
ECHA: Update Candidate List 27.06.2018
ECHA: Update Candidate list 15.01.2019
ECHA: Update candidate list 16.07.2019
ECHA: Update candidate list 16.01.2020
ECHA: Update candidate list 25.06.2020
ECHA: Update candidate list 19.01.2021
ECHA: Update candidate list 08.07.2021
ECHA: Update candidate list 17.01.2022
ECHA: Update candidate list 10.06.2022
ECHA: Update candidate list 17.01.2023
ECHA: Update candidate list 14.06.2023
ECHA: Update candidate list 23.01.2024