Regolamento (UE) 2017/745 MDR: Persona responsabile rispetto normativa - PR/PRRC
ID 9231 | 08.10.2019
Documento allegato sulla nuova Figura “Persona responsabile del rispetto della normativa” (PR o PRRC da Person Responsible for Regulatory Compliance), introdotta dal Regolamento (UE) 2017/745, (e Regolamento (UE) 2017/746 IDVR) con schemi di lettura individuazione e competenze.
Inserite le precisazioni della Guida MEDDEV MDCG 2019-7 Guidance on Article 15 of the Medical Device Regulation (MDR) and in vitro Diagnostic Device Regulation (IVDR) regarding a ‘person responsible for regulatory compliance’ (PRRC)
Excursus
Il nuovo Regolamento sui Dispositivi Medici Regolamento (UE) 2017/745 all'Art. 15 individua la "Persona responsabile del rispetto della normativa" (Person Responsible for Regulatory Compliance - PRRC)
Al Considerando (34) del Regolamento (UE) 2017/745 è riportata la ratio sulla Figura della PR:
"Si dovrebbe garantire che la supervisione e il controllo della fabbricazione dei dispositivi, nonché le attività di sorveglianza post-commercializzazione e di vigilanza a essi relative, siano effettuati all'interno dell'organizzazione del fabbricante da una persona responsabile del rispetto della normativa e in possesso di requisiti minimi di qualificazione".
Il Regolamento (UE) 2017/745 MDR interviene in modo incisivo su diversi aspetti chiave, dalle procedure di valutazione della conformità, alle indagini e alla valutazione clinica, alla vigilanza e la sorveglianza del mercato, introducendo al contempo disposizioni per garantire trasparenza e tracciabilità dei DM.
I fabbricanti debbono garantire e documentare un sistema per la gestione della qualità, ivi compreso il Post-Market Clinical Follow-up (PMCF).
La Persona responsabile del rispetto della normativa, dovrà possedere le competenze necessarie nel settore dei dispositivi medici per supportare il fabbricante di DM per tutti gli aspetti riguardanti la conformità normativa. Tale figura può essere interna o esterna, in relazione alla dimensione dell'Impresa.
Articolo 15 - Persona responsabile del rispetto della normativa
1. I fabbricanti, all'interno della loro organizzazione, dispongono di almeno una persona responsabile del rispetto della normativa che possieda le competenze necessarie nel settore dei dispositivi medici.
Le competenze necessarie sono attestate da una delle seguenti qualifiche:
a) un diploma, certificato o altro titolo ottenuto per aver completato studi universitari o un corso di studio riconosciuto equipollente dallo Stato membro in questione, in giurisprudenza, medicina, farmacia, ingegneria o un'altra disciplina scientifica pertinente, e almeno un anno di esperienza professionale nel campo della regolamentazione o dei sistemi di gestione della qualità relativi ai dispositivi medici;
b) quattro anni di esperienza professionale nel campo della regolamentazione o dei sistemi di gestione della qualità relativi ai dispositivi medici.
Fatte salve le disposizioni nazionali in materia di qualifiche professionali, i fabbricanti di dispositivi su misura possono dimostrare le competenze necessarie di cui al primo comma mediante il possesso di almeno due anni di esperienza professionale nel pertinente campo di fabbricazione.
2. Le microimprese e piccole imprese ai sensi della raccomandazione 2003/361/CE della Commissione non sono tenute ad avere la persona responsabile del rispetto della normativa all'interno della loro organizzazione ma sono tenute ad averla a disposizione in maniera permanente e continuativa.
3. La persona responsabile del rispetto della normativa ha il compito di assicurarsi almeno che:
a) la conformità dei dispositivi sia adeguatamente controllata conformemente al sistema di gestione della qualità in base al quale i dispositivi sono fabbricati prima del rilascio di un dispositivo;
b) la documentazione tecnica e la dichiarazione di conformità UE siano redatte e aggiornate;
c) siano soddisfatti gli obblighi di sorveglianza post-commercializzazione di cui all'articolo 10, paragrafo 10;
d) siano soddisfatti gli obblighi di segnalazione di cui agli articoli da 87 a 91;
e) nel caso di dispositivi oggetto di indagine, sia rilasciata la dichiarazione di cui all'allegato XV, capo II, punto 4.1.
4. Qualora più persone siano congiuntamente responsabili del rispetto della normativa, a norma dei paragrafi 1, 2 e 3, i rispettivi ambiti di competenza sono stabiliti per iscritto.
5. La persona responsabile del rispetto della normativa non subisce alcuno svantaggio all'interno dell'organizzazione del fabbricante in relazione alla corretta esecuzione dei propri compiti, indipendentemente dal fatto che sia o meno un dipendente dell'organizzazione.
6. I mandatari dispongono in maniera permanente e continuativa di almeno una persona responsabile del rispetto della normativa in possesso delle competenze necessarie nel campo della regolamentazione applicabile ai dispositivi medici nell'Unione.
Le competenze necessarie sono attestate da una delle seguenti qualifiche:
a) un diploma, certificato o altro titolo ottenuto per aver completato studi universitari o un corso di studio riconosciuto equipollente dallo Stato membro in questione, in giurisprudenza, medicina, farmacia, ingegneria o un'altra disciplina scientifica pertinente, e almeno un anno di esperienza professionale nel campo della regolamentazione o dei sistemi di gestione della qualità relativi ai dispositivi medici;
b) quattro anni di esperienza professionale nel campo della regolamentazione o dei sistemi di gestione della qualità relativi ai dispositivi medici.
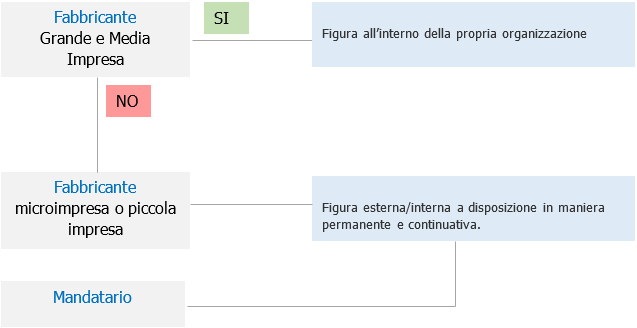
Il fabbricante ha l’obbligo di individuare la figura all’interno della propria organizzazione, per il mandatario e le micro/piccole imprese sarà sufficiente dimostrare che ne possono disporre in maniera permanente e continuativa, quindi possibile anche all'esterno dell'organizzazione.
Fig.1 - Individuazione della Figura PR
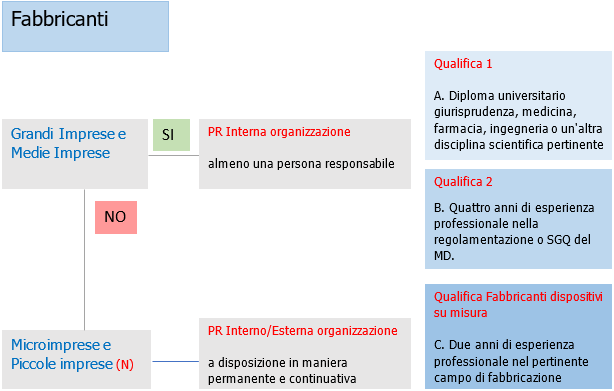
Qualifica PR necessarie nel settore dei dispositivi medici
Fig.2 - Qualifica Figura PR GI/MI/Micro/PI
La categoria delle microimprese delle piccole imprese e delle medie imprese (PMI) è costituita da imprese che occupano meno di 250 persone, il cui fatturato annuo non supera i 50 milioni di EUR oppure il cui totale di bilancio annuo non supera i 43 milioni di EUR.
Piccola impresa: un'impresa che occupa meno di 50 persone e realizza un fatturato annuo o un totale di bilancio annuo non superiori a 10 milioni di EUR.
Microimpresa: un'impresa che occupa meno di 50 persone e realizza un fatturato annuo o un totale di bilancio annuo non superiori a 10 milioni di EUR.
...
Guidance MDCG 2019-7
Guidance on Article 15 of the Medical Device Regulation (MDR) and in vitro Diagnostic Device Regulation (IVDR) regarding a ‘person responsible for regulatory compliance’ (PRRC)
...
Segue in allegato
Certifico Srl - IT | Rev. 00 2019
Copia autorizzata Abbonati