Mascherine e DPI: La Legge rilancio introduce la competenza regionale per la validazione in deroga
| ID 11211 | | Visite: 12901 | Documenti Riservati Marcatura CE | Permalink: https://www.certifico.com/id/11211 |
Mascherine e DPI: la Legge rilancio introduce la competenza regionale per la validazione in deroga (solo importazione)
ID 11211 | Rev. 2.0 del 09.10.2020 Documento completo allegato
______
Rev. 2.0 del 09.10.2020
In data 2 Ottobre 2020 INAIL ha pubblicato i Criteri semplificati di validazione in deroga alle norme vigenti per l'importazione e l'immissione in commercio dei DPI, definiti dal comitato tecnico appositamente istituito.
Con l'entrata in vigore dell'art. 66 bis del D.L. n. 34/2020, convertito con modificazioni dalla Legge n. 77/2020, è stata significativamente innovata la procedura di validazione straordinaria in deroga dei DPI. In particolare, per assicurare alle imprese il necessario fabbisogno dei dispositivi e sostenere la ripresa in sicurezza delle attività produttive, è stata prevista la definizione di criteri semplificati di validazione, in deroga alle norme vigenti, che assicurino l'efficacia protettiva, idonea all'utilizzo specifico, fino al termine dello stato di emergenza.
Il comitato tecnico, istituito ai sensi del comma 3 della medesima disposizione, ha definito tali criteri semplificati e li ha resi disponibili alle Regioni.
Rev. 1.0 del 05.08.2020 Documento completo allegato
Mascherine e DPI: La Legge rilancio Legge 17 luglio 2020 n. 77 (18 Luglio 2020) introduce la competenza regionale per la validazione in deroga per l’importazione, in particolare:
1. Validazione in deroga Mascherine e DPI competenza ISS/INAIL (per Produttori UE)
2. Validazione in deroga Mascherine e DPI Competenza Regioni (per Importatori)
______
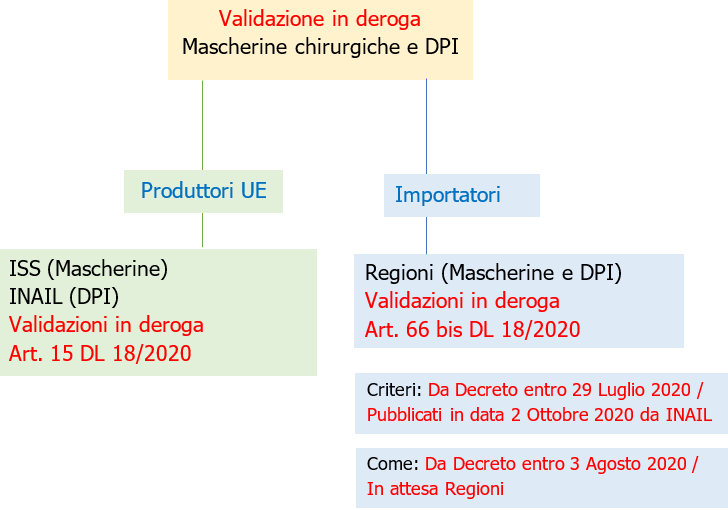
Validazione in deroga Mascherine e DPI separati se Produttori UE o Importatori
Riferimento Legge 17 luglio 2020 n. 77 in vigore dal 19/07/2020 (Conversione Decreto Legge Rilancio)
A. PRODUTTORI UE
L’ art. 66-bis della Legge 17 luglio 2020 n. 77, di conversione del decreto-legge 19 maggio 2020, n. 34, ha modificato le competenze dell’Iss e dell’Inail nella procedura di validazione straordinaria, con particolare riferimento all’importazione e all’immissione in commercio delle mascherine chirurgiche e dei dispositivi di protezione individuale, fino al termine dello stato di emergenza epidemiologica da Covid-19 (art. 15, co. 3).
L’Inail resta competente per la sola validazione delle richieste presentate dai produttori di dispositivi di protezione individuale (così come l’ISS per le mascherine chirurgiche), mentre per quelle presentate dagli importatori è previsto il passaggio alle regioni e la costituzione di un Comitato tecnico per la definizione di criteri semplificati di validazione, in deroga alle norme vigenti, che assicurino l'efficacia protettiva idonea all'utilizzo specifico.
A partire dal 4 agosto 2020, pertanto, le richieste di validazione straordinaria, ai sensi dell’articolo 15, co. 3, del decreto-legge 19 maggio 2020, n. 34, possono essere inoltrate all’Inail esclusivamente dai "produttori" con sede in un paese dell’Unione Europea.
Le modalità di presentazione online restano invariate.
B. IMPORTATORI
Con il nuovo Art. 66 bis. introdotto dalla Legge 17 luglio 2020 n. 77 - Conversione in legge, con modificazioni, del decreto-legge 19 maggio 2020, n. 34, recante misure urgenti in materia di salute, sostegno al lavoro e all'economia, nonche' di politiche sociali connesse all'emergenza epidemiologica da COVID-19. (GU n.180 del 18-07-2020 - S.O. n. 25), diventano di competenza regionale le modalità di presentazione delle domande di validazione delle mascherine chirurgiche e dei dispositivi di protezione individuale "importati" ai sensi del presente articolo, le Regioni individuano le strutture competenti per la medesima validazione.
1) Entro il 29 luglio 2020 sono definiti i criteri semplificati di validazione, in deroga alle norme vigenti, da apposito comitato ISS, ACCREDIA, UNI (Pubblicati il 2 Ottobre da INAIL).
2) Entro il 3 agosto le regioni definiscono le modalità di presentazione delle domande di validazione delle mascherine chirurgiche e dei dispositivi di protezione individuale. (In attesa dopoi 1))
Fig. 1 - Nuove procedure di validazione ed in deroga Mascherine chirurgiche e DPI alle norme vigenti
______
...
Art. 66-bis Disposizioni in materia di semplificazione dei procedimenti per l’importazione e la validazione di mascherine chirurgiche e dispositivi di protezione individuale
1. Al fine di assicurare alle imprese il necessario fabbisogno di mascherine chirurgiche e di dispositivi di protezione individuale e di sostenere la ripresa in sicurezza delle attività produttive, per l’importazione e l’immissione in commercio dei predetti dispositivi sono definiti criteri semplificati di validazione, in deroga alle norme vigenti, che assicurino l’efficacia protettiva idonea all’utilizzo specifico fino al termine dello stato di emergenza epidemiologica da COVID-19.
2. Per le mascherine chirurgiche i criteri di cui al comma 1 sono definiti entro dieci giorni dalla data di entrata in vigore della legge di conversione del presente decreto da un comitato tecnico composto da un rappresentante dell’Istituto superiore di sanità (ISS), che lo presiede, da un rappresentante designato dalle regioni, da un rappresentante dell’Ente italiano di accreditamento – ACCREDIA, da un rappresentante dell’Ente nazionale italiano di unificazione (UNI) e da un rappresentante degli organismi notificati indicato dalle associazioni degli organismi di valutazione della conformità socie dell’ACCREDIA. Il supporto amministrativo al comitato è assicurato dall’ISS. Ai componenti del comitato tecnico non spettano compensi, gettoni di presenza, rimborsi di spese o altri emolumenti comunque denominati.
3. Per i dispositivi di protezione individuale i criteri di cui al comma 1 sono definiti entro dieci giorni dalla data di entrata in vigore della legge di conversione del presente decreto da un comitato tecnico composto da un rappresentante dell’Istituto nazionale per l’assicurazione contro gli infortuni sul lavoro (INAIL), che lo presiede, da un rappresentante designato dalle regioni, da un rappresentante dell’ACCREDIA, da un rappresentante dell’UNI e da un rappresentante degli organismi notificati indicato dalle associazioni degli organismi di valutazione della conformità socie dell’ACCREDIA. Il supporto amministrativo al comitato è assicurato dall’INAIL. Ai componenti del comitato tecnico non spettano compensi, gettoni di presenza, rimborsi di spese o altri emolumenti comunque denominati.
4. Entro quindici giorni dalla data di entrata in vigore della legge di conversione del presente decreto, le regioni definiscono le modalità di presentazione delle domande di validazione delle mascherine chirurgiche e dei dispositivi di protezione individuale ai sensi del presente articolo e individuano le strutture competenti per la medesima validazione, in applicazione dei criteri di cui ai commi 1, 2 e 3, avvalendosi degli organismi notificati e dei laboratori di prova accreditati dall’ACCREDIA, nonché delle università e dei centri di ricerca e laboratori specializzati per l’effettuazione delle prove sui prodotti, e provvedono ai relativi controlli. Il monitoraggio sull’applicazione dei criteri semplificati di validazione è assicurato dai comitati di cui ai commi 2 e 3, che supportano l’attività delle regioni.
5. Restano ferme le validazioni in deroga effettuate dall’ISS e dall’INAIL in attuazione dell’articolo 15, commi 2 e 3, del decreto-legge 17 marzo 2020, n. 18, convertito, con modificazioni, dalla legge 24 aprile 2020, n. 27. L’ISS e l’INAIL rimangono competenti per la definizione delle domande pervenute ai predetti Istituti fino al quindicesimo giorno successivo alla data di entrata in vigore della legge di conversione del presente decreto, salvo che il richiedente rinunci espressamente a presentare domanda alla regione.
6. A decorrere dalla medesima data di cui al comma 5 del presente articolo, all’articolo 15 del decreto-legge 17 marzo 2020, n. 18, convertito, con modificazioni, dalla legge 24 aprile 2020, n. 27, sono apportate le seguenti modificazioni:
a) al comma 1, le parole: «, importare e immettere in commercio» sono soppresse;
b) al comma 2, le parole: «e gli importatori», ovunque ricorrono, e le parole: «e coloro che li immettono in commercio,» sono soppresse;
c) al comma 3:
1) al primo periodo, le parole: «, gli importatori» e le parole: «e coloro che li immettono in commercio» sono soppresse;
2) al secondo periodo, le parole: «e gli importatori» sono soppresse;
d) al comma 4, le parole: «e all’importatore è fatto divieto di immissione in commercio» sono soppresse.
7. Per tutta la durata dello stato di emergenza epidemiologica da COVID-19 resta fermo quanto disposto dall’articolo 5 -bis del decreto-legge 17 marzo 2020, n. 18, convertito, con modificazioni, dalla legge 24 aprile 2020, n. 27.
Non è più prevista la validazione in deroga delle mascherine chirurgiche e DPI all’ISS/INAIL per l’importazione e relativi obblighi importazione. Tale gestione diventa di competenza regionale.
// Modifica articolo 15 del decreto-legge 17 marzo 2020, n. 18 //:
Art. 15. Disposizioni straordinarie per la produzione di mascherine chirurgiche e dispositivi di protezione individuale
1. Fermo quanto previsto dall’articolo 5 -bis, per la gestione dell’emergenza COVID-19, e fino al termine dello stato di emergenza di cui alla delibera del Consiglio dei ministri in data 31 gennaio 2020, è consentito produrre, importare e immettere in commercio mascherine chirurgiche e dispositivi di protezione individuale in deroga alle vigenti disposizioni.
2. I produttori e gli importatori delle mascherine chirurgiche di cui al comma 1, e coloro che le immettono in commercio i quali intendono avvalersi della deroga ivi prevista, inviano all’Istituto superiore di sanità una autocertificazione nella quale, sotto la propria esclusiva responsabilità, attestano le caratteristiche tecniche delle mascherine e dichiarano che le stesse rispettano tutti i requisiti di sicurezza di cui alla vigente normativa. Entro e non oltre 3 giorni dall’invio della citata autocertificazione, i produttori e gli importatori devono altresì trasmettere all’Istituto superiore di sanità ogni elemento utile alla validazione delle mascherine chirurgiche oggetto della stessa. L’Istituto superiore di sanità, nel termine di 3 giorni dalla ricezione di quanto indicato nel presente comma, si pronuncia circa la rispondenza delle mascherine chirurgiche alle norme vigenti.
3. I produttori, gli importatori dei dispositivi di protezione individuale di cui al comma 1 e coloro che li immettono in commercio, i quali intendono avvalersi della deroga ivi prevista, inviano all’INAIL una autocertificazione nella quale, sotto la propria esclusiva responsabilità, attestano le caratteristiche tecniche dei citati dispositivi e dichiarano che gli stessi rispettano tutti i requisiti di sicurezza di cui alla vigente normativa. Entro e non oltre 3 giorni dall’invio della citata autocertificazione, i produttori e gli importatori devono altresì trasmettere all’INAIL ogni elemento utile alla validazione dei dispositivi di protezione individuale oggetto della stessa. L’INAIL, nel termine di 3 giorni dalla ricezione di quanto indicato nel presente comma, si pronuncia circa la rispondenza dei dispositivi di protezione individuale alle norme vigenti.
4. Qualora all’esito della valutazione di cui ai commi 2 e 3 i prodotti risultino non conformi alle vigenti norme, impregiudicata l’applicazione delle disposizioni in materia di autocertificazione, il produttore ne cessa immediatamente la produzione e all’importatore è fatto divieto di immissione in commercio.
...
segue in allegato
Certifico Srl - IT | Rev. 2.0 2020
©Copia autorizzata Abbonati
Matrice Revisioni
| Rev. | Data | Oggetto | Autore |
| 2.0 | 09.10.2020 | Criteri semplificati INAIL | Certifico Srl |
| 1.0 | 05.08.2020 | Correzioni e integrazioni | Certifico Srl |
| 0.0 | 19.07.2020 | --- | Certifico Srl |
Collegati
Legge 17 luglio 2020 n. 77
Decreto-Legge 19 maggio 2020 n. 34
Decreto Legge 17 marzo 2020 n. 18
Legge 24 aprile 2020 n. 27
| Descrizione | Livello | Dimensione | Downloads | |
|---|---|---|---|---|
| Mascherine chirurgiche e DPI Validazione ed in deroga - Regioni Rev 2.0 2020.pdf Certifico S.r.l. Rev. 2.0 2020 |
448 kB | 77 | ||
| Mascherine chirurgiche e DPI Validazione ed in deroga - Regioni Rev. 1.0 2020.pdf Certifico S.r.l. Rev. 1.0 2020 |
442 kB | 47 | ||
| Mascherine chirurgiche e DPI Validazione ed in deroga - Regioni Rev. 00 2020.pdf Certifico S.r.l. Rev. 00 2020 |
427 kB | 95 |